Manejo da mulher na menopausa
Menopausa implica uma nova visão clínica de pacientes do sexo feminino.
Artigo publicado no site do Fleury Medicina e Saúde.
Definida como a etapa em que a mulher passa da fase reprodutiva para a não reprodutiva, a transição menopausal caracteriza-se pelas primeiras manifestações clínicas do declínio hormonal, com redução fisiológica da função ovariana e alterações endócrinas, metabólicas, psíquicas e somáticas que podem comprometer a qualidade de vida. A menopausa, por sua vez, é a data da última menstruação.
Nesta oportunidade, vamos tratar não apenas do diagnóstico da condição em circunstâncias normais, por volta do início da quinta década de vida, como também de seu contraponto clínico, a insuficiência ovariana precoce.
Uma vez constatado o diagnóstico clínico e laboratorial da menopausa, a mulher deve realizar uma propedêutica mínima para a manutenção de sua saúde, que inclui a avaliação de mamas, trato genital inferior, massa óssea e tiroide, além de condições que impactam o coração, como diabetes e dislipidemias.
Em vista disso, o presente guia aborda esses temas e também o rastreamento do câncer de mama na mulher durante a menopausa e a investigação do sangramento anormal nessa fase, o qual pode ser decorrente de alterações orgânicas, distúrbios menstruais ou neoplasias, como o adenocarcinoma de endométrio e o câncer de colo de útero.
Diagnóstico clínico e laboratorial da menopausa
A prevalência dos sintomas típicos da transição menopausal varia, entre as mulheres, de 22% a 75% e depende da etnia e da localização geográfica. No Brasil, a menopausa ocorre, em média, em torno dos 50 anos.
| Sintomas neurovegetativos, neuropsíquicos ou genitais próprios da transição menopausal | |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
FSH: hormônio foliculoestimulante; AMH: hormônio antimülleriano; USTV: ultrassonografia pélvica transvaginal.
Obs.: na propedêutica mínima, a ultrassonografia pélvica deve ser feita, de preferência, por via transvaginal.
(1) No período de transição menopausal até a menopausa, pode haver grande variação dos níveis hormonais. Não são infrequentes concentrações elevadas de FSH em um momento e, em dosagens subsequentes, dentro da normalidade. É possível que o mesmo ocorra com o estrogênio, que pode estar alto, normal ou baixo nesse período.
Rastreamento do câncer de mama na mulher na menopausa
A incidência do câncer de mama na população feminina aumenta com o avanço da idade. Atualmente, cerca de dois terços das neoplasias mamárias ocorrem acima dos 50 anos e, portanto, a informação e a conscientização das mulheres menopausadas sobre a importância do diagnóstico precoce da doença são fundamentais.
Com o objetivo de detectar pequenos tumores assintomáticos, o rastreamento da neoplasia tem impacto comprovado na queda da mortalidade por essa causa, além de reduzir a extensão do tratamento cirúrgico e a necessidade de quimioterapia, bem como de aumentar a sobrevida da paciente.
Recomendações para mulheres entre 40 e 69 anos
Nessa faixa etária, preconiza-se a mamografia para todas as pacientes, com periodicidade anual. Já a ultrassonografia de mamas pode ser considerada individualmente em mulheres com tecido mamário denso, como adjuvante à mamografia, e naquelas com alto risco, nas quais o rastreamento por ressonância magnética (RM) está indicado, mas não pode ser realizado por qualquer razão.
Grupos de maior risco e recomendações da Febrasgo, do Colégio Brasileiro de Radiologia e da Sociedade Brasileira de Mastologia
| Mamografia | RM | |
| Mutação em genes com suscetibilidade para câncer de mama e familiares de primeiro grau não testadas | Anual, com início aos 30 anos | Anual, com início aos 25 anos |
| Forte história familiar (lifetime risk ?20%) |
Anual, dez anos antes da idade do familiar mais jovem ao diagnóstico de câncer de mama, mas não antes dos 30 anos, para mamografia, e dos 25 anos, para RM | |
| Irradiação torácica antes dos 30 anos |
Anual, com início oito anos após o término da radioterapia, mas não antes dos 30 anos, para a mamografia, e dos 25 anos, para RM | |
| História pessoal de câncer de mama, neoplasias lobulares e hiperplasia ductal atípica | Anual, a partir do diagnóstico | |
Recomendações para mulheres com mais de 70 anos
Sugere-se que, nessa faixa etária, a decisão sobre a continuidade do rastreamento seja individual, considerando-se a saúde global e a longevidade estimada da paciente. Isso porque alguns fatos indicam que o benefício do rastreamento mamográfico pode diminuir nesse grupo, em vista da menor expectativa de vida, da maior frequência de tumores com bom prognóstico e do maior risco de óbito por outras doenças.
Rastreamento mamográfico das mulheres com mais de 70 anos
| Mulheres com expectativa de vida maior que sete anos, com base nas comorbidades | Anualmente |
| Mulheres em condições de ser submetidas a uma investigação diagnóstica invasiva e a tratamento após um resultado anormal do rastreamento | Anualmente |
Adaptado de: Rev Bras Mastologia. 2013; 23(1):5-11.
Quando a menopausa é precoce
Insuficiência ovariana primária
Com incidência estimada de 1:100 mulheres, a insuficiência ovariana primária (IOP) se caracteriza por oligomenorreia ou amenorreia secundárias por mais de três meses em mulheres com menos de 40 anos e níveis elevados de gonadotrofinas, o que leva ao hipogonadismo e até à infertilidade. Apesar de ter causas múltiplas [tabela], a patogênese da IOP está associada a uma redução congênita no número de folículos primordiais, a um recrutamento pobre dos folículos ou a uma apoptose folicular acelerada.
Na avaliação clínica inicial do quadro, recomendam-se a USTV e a dosagem do FSH [algoritmo]. O cariótipo por banda G deve ser solicitado, uma vez que as causas genéticas e cromossômicas correspondem a uma parcela importante das etiologias. Outros exames genéticos e imunológicos podem ser pedidos individualmente. Em mulheres que ainda pretendem engravidar, o estudo da reserva ovariana é essencial e deve incluir a contagem de folículos antrais à ultrassonografia e a dosagem do AMH [boxe].
No entanto, a função ovulatória pode apresentar períodos de retomada espontânea em até 25% dos casos, tanto é assim que cerca de 5% das mulheres com mais de um ano de diagnóstico têm chance de engravidar espontaneamente. Nesse cenário, é muito importante a pesquisa de mutação do gene FMR1, que causa a síndrome do X frágil, pois, se presente, há risco de transmissão da alteração para um filho do sexo masculino, o que ocasiona potencialmente um quadro mais grave, com deficiência intelectual. O teste utiliza a PCR para a pesquisa do X frágil.
| Causas não iatrogênicas mais comuns associadas à IOP |
| Genéticas Síndrome de Turner; pré-mutação do gene FMR1; outras |
| Metabólicas Deficiência da galactose-1-fosfato uridiltransferase; síndrome da glicoproteína deficientes em carboidratos; outras |
| Autoimunes Síndrome poliglandular autoimune; hipotiroidismo; diabetes mellitus tipo 1; miastenia gravis; lúpus eritematoso sistêmico; doença de Addison; púrpura trombocitopênica; artrite reumatoide; doença de Crohn; vitiligo; alopecia; anemia perniciosa ou autoimune; síndrome de Sjögren; outras |
| Infecciosas Infecções virais; tuberculose; malária; outras |
| Outras |
| Causas genéticas As alterações que envolvem o cromossomo X estão entre as principais causas genéticas de IOP |
|
Papel do hormônio antimülleriano
O AMH é uma glicoproteína produzida, nas mulheres, pelas células da granulosa dos folículos ovarianos pré-antrais e antrais pequenos, que reflete, indiretamente, o número de folículos remanescentes no ovário, com a vantagem de não apresentar variações importantes durante o ciclo menstrual. Dessa forma, tem utilidade na avaliação da reserva ovariana, na investigação da função dessa gônada e da transição menopausal. Nas pacientes usuárias de contraceptivo oral por tempo prolongado e nas mulheres que apresentam deficiência de vitamina D, as concentrações do AMH caem cerca de 20%.
Algoritmo para diagnóstico inicial de IOP
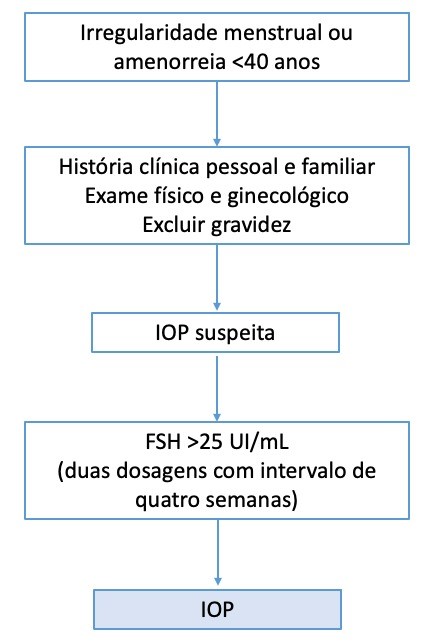
Adaptado de: N. Mendoza et al. Maturitas 80 (2015) 220-225.
Sangramento vaginal anormal na menopausa
O exame de primeira linha na investigação do sangramento vaginal anormal em mulheres menopausadas é a ultrassonografia, de preferência por via transvaginal. Se constatado o espessamento do eco endometrial, deve-se prosseguir a pesquisa com a histeroscopia e a biópsia de endométrio, a fim de descartar a neoplasia endometrial.
O diagnóstico do câncer de endométrio exige a biópsia e o estudo anatomopatológico. Atualmente, a histeroscopia diagnóstica configura o método de escolha para a obtenção da amostra de tecido endometrial, uma vez que possibilita a execução de biópsia dirigida sob visão histeroscópica, além de permitir a visualização de toda a cavidade uterina, assim como a avaliação da extensão das lesões endometriais e do acometimento do canal endocervical.
A RM tem importância no estadiamento dos casos positivos para carcinoma de endométrio, mas não para o diagnóstico, visto que não diferencia um espessamento benigno de um maligno.
O adenocarcinoma de endométrio
O câncer endometrial está entre as neoplasias malignas do trato genital feminino mais frequentes em países desenvolvidos. Mais de 90% dos casos ocorrem em mulheres acima de 50 anos, contribuindo para 1% a 2% de todas as causas de morte por neoplasia. No Brasil, é a segunda doença maligna do trato genital mais frequente nas mulheres – a primeira ainda continua sendo o tumor de colo uterino.
O risco de apresentar adenocarcinoma de endométrio atualmente chega a 2,8% (1:41 mulheres), o qual, contudo, está em ascensão devido ao envelhecimento populacional, ao uso de terapias estrogênicas prolongadas, sem oposição por progestágenos, e a condições como síndromes dos ovários policísticos, tumores produtores de estrogênios, nuliparidade, ciclos menstruais irregulares, idade precoce de menarca, idade tardia de menopausa, obesidade, diabetes mellitus tipo 2 e hipertensão arterial.
O sintoma mais comum da neoplasia é o sangramento vaginal anormal, visto em aproximadamente 95% dos casos, que sempre deve ser investigado. Afinal, se diagnosticada logo após o início dessa manifestação, a doença fica restrita ao útero em mais de 75% dessas pacientes e, portanto, em estágio inicial, com prognóstico favorável e altas taxas de cura por meio de cirurgia e, eventualmente, radioterapia associada.
Roteiro para investigação da neoplasia de endométrio
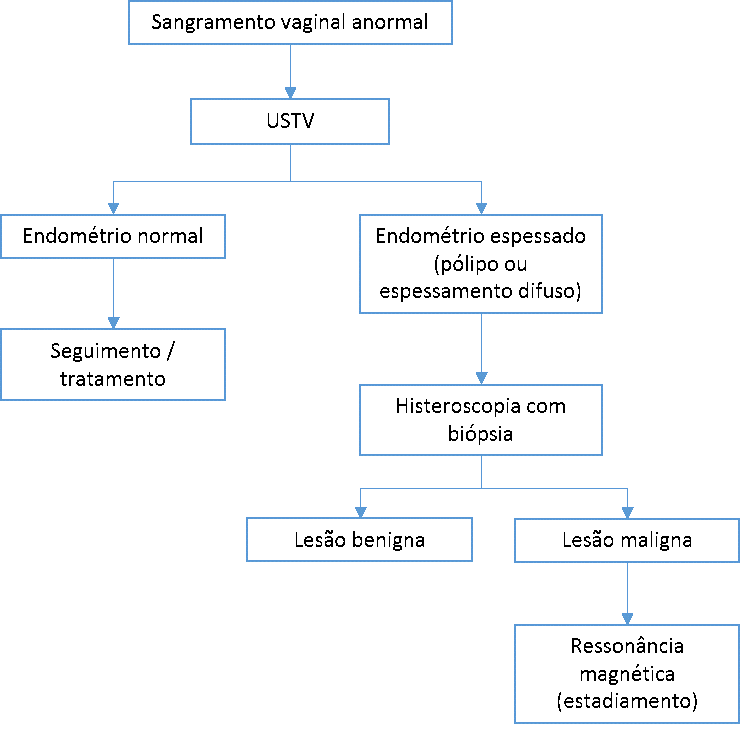
Osteoporose na mulher
O diagnóstico de osteopenia/osteoporose geralmente se dá pela determinação dos valores de densidade mineral óssea (DMO) obtidos pela densitometria óssea, mas, por se tratar de uma condição silenciosa, muitas vezes só se detecta sua presença quando há fratura. Vale ressaltar que o diagnóstico clínico de osteoporose pode ser feito na presença de fratura por fragilidade (especialmente fratura vertebral e de quadril) nas mulheres na pós-menopausa independentemente dos valores de DMO. O sexo feminino configura um fator de risco para a doença. A osteoporose pode estar presente em cerca de 20% a 30% das mulheres na pós-menopausa.
Fatores de risco
| Não modificáveis | Modificáveis |
| • Presença de fratura prévia • Idade avançada • Sexo feminino • História familiar de osteoporose (em parentes de primeiro grau) • Etnia caucasiana e asiática • Baixo pico de massa óssea |
• Etilismo • Tabagismo • Sedentarismo • Ingestão inadequada de cálcio e de vitamina D • Baixo índice de massa corporal (<21 kg/m²) • Hipogonadismo • Deficiência estrogênica |
Doença primária versus secundária
A osteoporose pode ser classificada em primária ou secundária. A forma mais comum é a primária, relacionada à redução dos níveis de estrogênio da pós-menopausa ou ao envelhecimento, etiologia que deve ser considerada desde que outros agentes causadores tenham sido afastados (osteoporose secundária). Muitas doenças estão associadas com a osteoporose secundária, contudo a principal causa é a induzida por glicocorticoides. Há, porém, outras etiologias frequentes, como hipogonadismo, hipertiroidismo, anorexia nervosa, hiperparatiroidismo, síndromes de má absorção, deficiência de cálcio e de vitamina D, alcoolismo, hipercalciúria, além de tratamento crônico com tiroxina em excesso, anticonvulsivantes, agonistas de GnRH ou inibidores de aromatase, por exemplo.
Avaliação laboratorial da osteoporose
Para descartar as causas secundárias de osteoporose, as Diretrizes Brasileiras para o Diagnóstico e Tratamento da Osteoporose em Mulheres na Pós-Menopausa recomendam uma triagem inicial mínima com hemograma, cálcio total, fósforo e fosfatase alcalina, TSH, 25-OH-vitamina D, calciúria de 24 horas e creatinina. Outros exames devem ser solicitados de acordo com a suspeita clínica.
Densitometria óssea
Na densitometria, deve-se utilizar o menor T-score entre os sítios avaliados: coluna lombar (L1-L4), colo femoral e fêmur total. O rádio 33% pode ser usado como complementação ou na impossibilidade de avaliar os sítios mencionados. Segundo a International Society for Clinical Densitometry (ISCD), a avaliação da DMO é recomendada em mulheres com idade ?65 anos ou antes, naquelas com antecedente de fratura por fragilidade, baixo peso ou uso de medicações/doenças relacionadas à redução de massa óssea.
Critérios diagnósticos de osteopenia e osteoporose pela densitometria óssea
| Mulheres na pós-menopausa | |
| Classificação | T-score* |
| Normal | ?-1,0 desvio-padrão (DP) |
| Osteopenia | De -1,1 a -2,4 DP |
| Osteoporose | ?-2,5 DP |
| Mulheres na pré-menopausa (20 anos até a menopausa) | |
| Classificação | Z-score |
| Massa óssea dentro do esperado para a idade cronológica | >-2,0 DP |
| Massa óssea abaixo do esperado para a idade cronológica | ?-2,0 DP |
*Pode ser utilizado também para as mulheres na transição menopausal.
Avaliação de fratura vertebral por densitometria
A investigação da presença de fratura vertebral deve ser considerada em pacientes de maior risco porque mais da metade dessas fraturas podem ser assintomáticas. É possível fazer o rastreamento por meio de raios X de coluna torácica e lombar ou da avaliação de fratura vertebral por DXA – Vertebral Fracture Assessment (VFA). Essa técnica utiliza radiação mais baixa que a radiografia convencional, pode ser feita no mesmo momento da densitometria e possui capacidade similar à da radiografia para identificar fraturas vertebrais moderadas e graves.
Indicações para realizar avaliação de fratura vertebral (VFA) por densitometria (ISCD)
| Portadores de osteopenia ou osteoporose e um ou mais dos seguintes critérios: |
| Mulheres com 70 anos ou mais |
| Homens com 80 anos ou mais |
| Redução de altura em mais de 4 cm (altura aos 25 anos – altura atual) |
| Relato de fratura vertebral não documentada por método de imagem |
| Uso crônico de corticoide (5 mg de prednisona ou equivalente por três meses ou mais) |
Fracture Risk Assessment Tool (FRAX)
A combinação de fatores de risco clínicos com a avaliação da DMO por DXA é recomendada para melhor estratificar o risco de fraturas nos indivíduos sem diagnóstico clínico ou densitométrico de osteoporose (já classificados como alto risco). Para tanto, existe uma ferramenta gratuita denominada FRAX, que calcula a probabilidade, em valor absoluto, da ocorrência de uma fratura osteoporótica maior (vértebra, quadril, antebraço e úmero) e de fratura de quadril nos próximos dez anos, de acordo com o país selecionado. Uma vez calculada essa probabilidade pelo FRAX, é necessário inserir os valores na curva de limite de intervenção do National Osteoporosis Guideline Group (NOGG). Basta acessar o site: https://abrasso.org.br/calculadora/calculadora.
Trabecular Bone Score (TBS)
Trata-se de uma ferramenta que avalia indiretamente a qualidade óssea por meio da distribuição dos pixels da imagem de coluna lombar adquirida por DXA, sem radiação adicional. Essa medida se relaciona à deterioração da microarquitetura óssea e ao risco de fraturas, de modo independente da DMO e dos fatores de risco clínicos, podendo ser incorporada à calculadora FRAX.
Vitamina D
A dosagem de vitamina D precisa ser realizada pela mensuração da concentração sérica de 25-hidroxivitamina D (25-OH-D), pois reflete a vitamina obtida por meio da ingestão alimentar e da exposição à luz solar. Sua forma ativa, a 1,25(OH)2D, não fornece informação fidedigna sobre a quantidade do nutriente no organismo, uma vez que, quando há déficit dessa vitamina, o paratormônio se eleva, o que aumenta a atividade renal da 1-?-hidroxilase, promovendo a conversão da 25(OH)D em 1,25(OH)2D.
A mensuração da vitamina D está indicada nos pacientes que pertencem ao grupo de risco para hipovitaminose D, com base em dados de história clínica, exame físico e testes complementares. Não há evidências de benefícios do uso da dosagem em população adulta sem comorbidades, ou seja, o rastreamento populacional indiscriminado não é preconizado.
Grupos de risco para hipovitaminose D
| – Idosos (acima de 60 anos) – Indivíduos que não se expõem ao sol ou que tenham contraindicação à exposição solar – Indivíduos com fraturas ou quedas recorrentes – Gestantes e lactantes – Pacientes com osteoporose (primária e secundária) – Portadores de doenças osteometabólicas (raquitismo, osteomalacia e hiperparatiroidismo) |
– Pacientes com doença renal crônica, diabetes, neoplasias malignas, sarcopenia ou obesidade – Portadores de síndromes de má absorção (pós-cirurgia bariátrica e doença inflamatória intestinal) – Usuários de medicações que possam interferir na formação e na degradação da vitamina D, como terapia antirretroviral, glicocorticoides e anticonvulsivantes |
Valores de referência da dosagem de 25(OH)D:
– População saudável (até 60 anos): acima de 20 ng/mL*
– Deficiente: inferior a 20 ng/mL
– Risco de toxicidade/hipercalcemia: acima de 100 ng/mL
*Valores entre 30 a 60 ng/mL são desejáveis na população acima de 60 anos, gestantes, lactantes, pacientes com raquitismo/osteomalacia, com osteoporose e com história de quedas e fraturas, causas secundárias de osteoporose, como doenças e medicações, hiperparatiroidismo, doenças inflamatórias, doenças autoimunes, doença renal crônica e síndromes de má absorção (clínicas ou pós-cirúrgicas).
Referência:
Posicionamento Oficial da Sociedade Brasileira de Patologia Clínica/Medicina Laboratorial (SBPC/ML) e da Sociedade Brasileira de Endocrinologia e Metabologia (SBEM) – Intervalos de Referência da Vitamina D-25(OH)D. https://www.endocrino.org.br/vitamina-d-novos-valores-de-referencia; http://www.sbpc.org.br/noticias-e-comunicacao/novos-intervalos-de-referencia-de-vitamina-d.
Veiculado em 2014/11/20
